【特康特食】4月20日世界高尿酸血症日 "关爱高尿酸人群营养与健康"
发表时间:2023-04-20

一、高尿酸血症和痛风的流行病学
痛风是同遗传有关的嘌呤代谢紊乱或与尿酸排泄减少有关所引起的一组代谢性疾病。其临床特点为反复发作的急性关
节炎、高尿酸血症、尿路结石、肾尿酸结石,严重者导致关节强直或畸形、肾实质损害等。痛风发病的关键生化基础是高
尿酸血症(HUA)。研究表明,约有5%~19%的HUA会发展为痛风[1]。
1.高尿酸血症和痛风发病率
痛风在亚洲被视为一种罕见疾病,而在欧美地区则是一种常见疾病,随着人们饮食结构的变化,高蛋白、高嘌呤食物
摄入量日益增多,高尿酸血症和痛风在我国也逐渐成为常见疾病。 2013年我国HUA患病率男性约为16.85%~18.32%,
女性约为7.88%~9.30%,痛风患病率男性约为0.83%~1.98%,女性约为0.07%~0.72%,较以前明显上升[2]。
据中国疾病控制中心报告,全国高尿酸血症患者超过8000万,比15年前增加了15~30倍,预计2020年中国痛风患者将跨越1亿[3]。
2.高尿酸血症和痛风的分布特点
(1)年龄差异
高尿酸血症、痛风与年龄因素具有重大的关联。中老年人为原发性痛风的高发群体,44岁为平均发病年龄[5]。但近几年来,
发病年龄趋于年轻化,2014年的调查结果显示20~30岁的年轻人占据此病症群体的64%。
(2)性别差异
男性痛风发病率显著高于女性,其原因主要为男性体内的雄激素可促进肾脏重吸收尿酸而抑制尿酸排泄,而女性体内的17β
-雌二醇可以调节尿酸代谢及嘌呤生物合成过程,从而降低尿酸水平[6]。
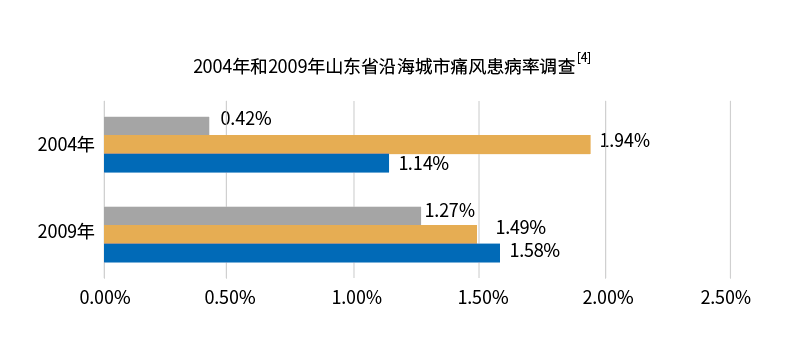
(3)地区差异
2015年《国际内分泌代谢杂志》指出82%的人群因地理位置患有此种病症,我国大多数流行病学研究也发现,沿海地区
痛风与高尿素血症的发病率高于内陆地区,主要原因为当地居民海产品摄入量明显高于内地[7]。
3.病因及发病机制
痛风的直接原因是高尿酸血症。当高尿酸血症患者出现尿酸盐结晶沉积、关节炎和(或)肾病、肾结石等时,才称为痛风[8]。痛风可分为原发性痛风和继发性痛风两大类。
(1)原发性痛风
原发性痛风大多为先天遗传性。遗传特点为X连锁隐性遗传,女性为携带者,男性发病[6]。其原因是多方面的,以下面两个方面为主:
① 尿酸清除减少
这类患者约占痛风的90%,临床检查可发现其尿酸的清除能力明显低于正常人,70%~80%的患者显示肾脏功能不全,总体表现为痛风患者存在肾脏的尿酸代谢功能紊乱。
② 尿酸产生过多
由先天性嘌呤代谢障碍引起的,主要是尿酸酶基因失活以及尿酸合成过程中关键酶的基因缺陷,如次黄嘌呤-鸟嘌呤磷酸核糖转移酶缺乏、磷酸核糖焦磷合成酶活性增高。
(2)继发性痛风[9]
继发于其他疾病,包括遗传性疾病、获得性疾病或药物,主要由于肾脏疾病导致尿酸排泄减少,骨髓增生性疾病及放疗至尿酸生成增多,某些药物抑制尿酸的排泄等多种原因所致。
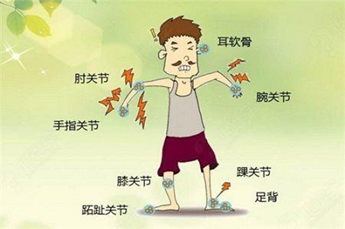
二、高尿酸血症和痛风的临床症状
1.无症状期
此期仅有尿酸的持续性或波动性增高,但无关节炎、痛风石、肾结石等临床表现,有些可终生不出现症状。
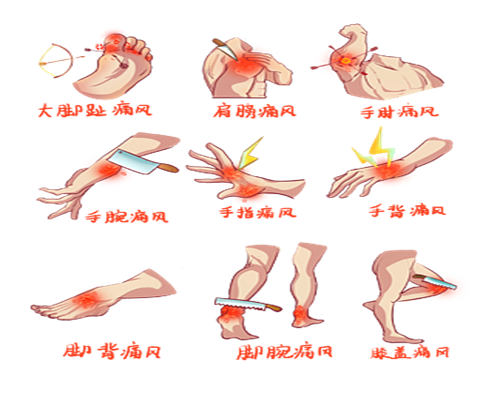
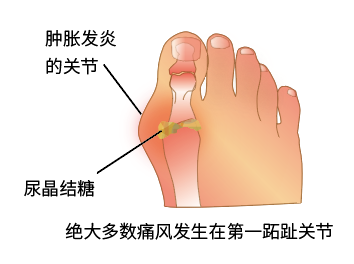
2.急性期
以急性关节炎为主要临床表现,典型症状的特点是骤然起病,最常侵犯的部位是第一跖趾,
数小时内出现受累关节的红、肿、热、痛和功能障碍,病程持续时间可在数小时或数日不等。
3. 间歇期
两次发作之间的一段静止期。大多数患者一生会发作多次,间隔时间可为6个月至1年,甚至5~10年不等。未进行治疗发作次数会越来越频繁。
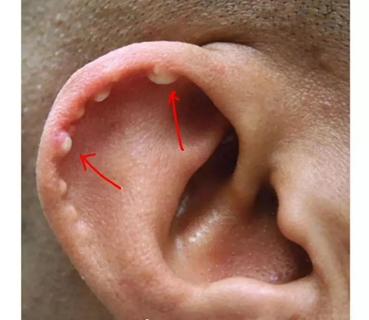
4. 慢性期
主要临床表现为痛风石、慢性关节炎、尿路结石和肾炎等。
5. 高尿酸血症和痛风的临床诊断
高尿酸血症和痛风的检查手段主要有血尿酸测定、尿尿酸测定、关节液或痛风石内容物检查、X线检查、电子计算机X线体层显像(CT)与磁共振显像(MRI)检查以及超声检查。
男性和绝经后女性血尿酸>420μmol/L(7.0mg/dl)、绝经前女性>358μmol/L(6.0mg/dl)可诊断为高尿酸血症。
如出现特征性关节炎表现、尿路结石或肾绞痛发作,伴有高尿酸血症应考虑痛风,关节液穿刺或痛风石活检发现尿酸盐结晶可确诊痛风[12]。
三、高尿酸血症和痛风的治疗方法
痛风治疗目标是控制急性关节炎发作及复发、预防尿酸盐沉积、促进痛风石吸收、防止慢性关节炎进展、防止尿酸性肾结石、痛风性肾病及肾功能损害。患者教育、适当的生活方式和饮食习惯是痛风长期治疗的基础。

1. 饮食治疗
(1)限制嘌呤:病人应长期控制嘌呤摄入,选用低嘌呤食物,禁用高嘌呤食物。
(2)限制热能:一般为1500~1800kcal,切忌减重过快,应循序渐进。
(3)蛋白质:应以植物蛋白为主,动物蛋白可选用牛奶、鸡蛋。
(4)供给充足B族维生素和维生素C。
(5)禁用强烈香料及调味品,如酒和辛辣调味品。
(6)每日饮水应在2000ml以上,最好能达到3000ml,慎用抑制尿酸排泄的药物[13]。
2. 急性痛风关节炎治疗
秋水仙碱、非甾体抗炎药(NSAIDs)和糖皮质激素是急性痛风性关节炎治疗的一线药物。
急性发作期不进行降尿酸治疗,但已服用降尿酸药物者不需停用,以免引起尿酸波动,导致发作时间延长或再次发作。
3. 间歇期和慢性痛风关节炎治疗
采用降尿酸药物治疗,目标是血尿酸浓度低于6mg/dl,以减少或清除体内沉积的尿酸盐结晶。降尿酸药物应在急性发作缓解后从小剂量开始,逐渐加量,并根据血尿酸调整至最小有效剂量长期甚至终身维持。
(1)抑制尿酸合成药物:别嘌醇、非布司他
(2)促进尿酸排泄药物:丙磺舒、苯溴马隆
(3)尿酸酶
在开始降尿酸治疗时,推荐同时服用秋水仙碱0.5~1mg/d或小剂量NSAIDs1~12个月,以预防急性痛风发作。
4. 痛风肾脏病变治疗
应选用抑制尿酸合成药物,同时碱化尿液,保持尿量。其他处理同慢性肾炎,如出现肾功能不全,可行透析治疗,必要时可做肾移植。
5. 伴发疾病治疗
痛风常伴发代谢综合征,如高血压、高脂血症、肥胖症、2型糖尿病等,应积极治疗上述伴发疾病。
6. 无症状高尿酸血症治疗
以饮食治疗为主,一般不推荐使用降尿酸药物。如经饮食控制血尿酸仍高于9mg/dl或血尿酸高于8mg/dl并有家族史或伴发相关疾病的患者,可考虑降尿酸治疗
7. 手术治疗
必要时可选择剔除痛风石、对残毁关节进行矫形等手术治疗[14]。
四、高尿酸血症和痛风患者的营养代谢和营养需求
1.营养代谢特点
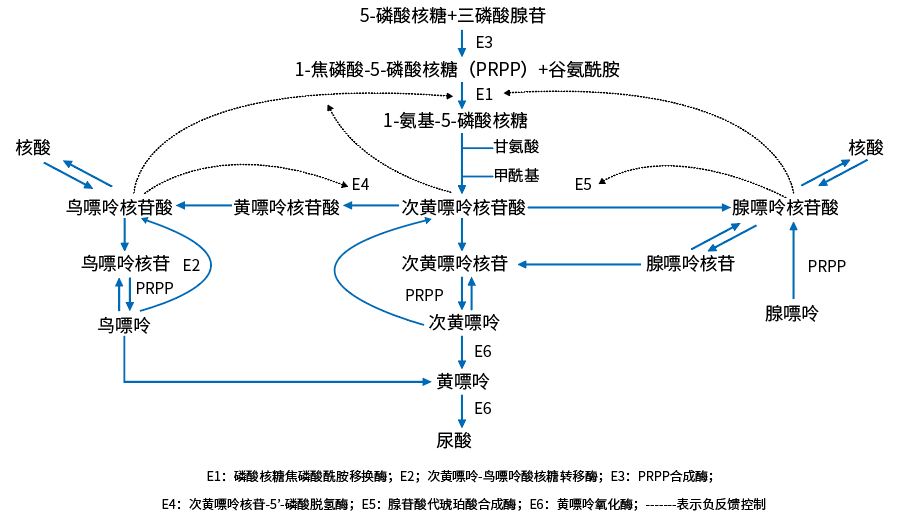
嘌呤代谢的终产物主要由细胞代谢分解的核酸和其他嘌呤类化合物,以及食物中的嘌呤经酶的作用分解而来。人体中尿酸80%来源于内源性嘌呤代谢,20%来源于富含嘌呤或核酸蛋白食物。
实际上食物来源的嘌呤和嘧啶很少被机体利用。但痛风患者由于存在嘌呤代谢有关酶的异常,可利用外源性嘌呤通过合成补救途径使嘌呤核苷酸合成增加,然后再体内分解产生尿酸。
高蛋白、高嘌呤的摄入也可通过腺苷三磷酸(ATP)分解加速。ATP分解可形成腺苷二磷酸、腺苷一磷酸、一磷酸次黄嘌呤核苷酸、一磷酸黄嘌呤核苷酸等,最后在黄嘌呤氧化酶作用下生成尿酸。
有研究表明,大量饮酒可使参与机体氧化还原反应的重要辅酶烟酰胺腺嘌呤二核苷酸(NADH)大量消耗,使ATP生成障碍,而加速其分解,使血尿酸升高引发痛风。
B族维生素和维生素C可促进组织沉积的尿酸盐溶解,有利于缓解痛风[15]。
2. 营养需求:
痛风患者不能采用正常人膳食,需要避免进食动物内脏、含糖饮料和酒,限制肉、海鲜和甜点的摄入。
痛风多为肥胖患者,且大多数痛风患者具有长期饮食和作息不规律,吸烟,酗酒等不良生活习惯,易造成饮食不均衡,进一步形成营养不良。
痛风患者饮食中应注意限制高嘌呤食物的摄入,但如果盲目忌口,同样会造成营养失衡,不利于防止和延缓急性痛风的发作。
因此,对痛风患者采用合理、均衡、科学的长期膳食干预在痛风整个病程中极其重要。
五、高尿酸血症和痛风患者的营养干预
高尿酸血症和痛风患者营养支持、治疗专家共治&指南
1、痛风及高尿酸血症基层诊疗指南(2019年)(中华医学会 中华医学会全科医学分会)
2、中国高尿酸血症与痛风诊疗指南(2019)(中华医学会内分泌学分会)
3、2016中国痛风诊疗指南(中华医学会风湿病学分会)
4、高尿酸血症和痛风治疗的中国专家共识(中华医学会内分泌学分会)
5、中国慢性肾脏病患者合并高尿酸血症诊治专家共识(中国慢性肾脏病患者合并高尿酸血症诊治共识专家组)
6、中国高尿酸血症相关疾病诊疗多学科专家共识(高尿酸血症相关疾病诊疗多学科共识专家组)
《2016中国痛风诊疗指南》指出,痛风患者应遵循下述原则:
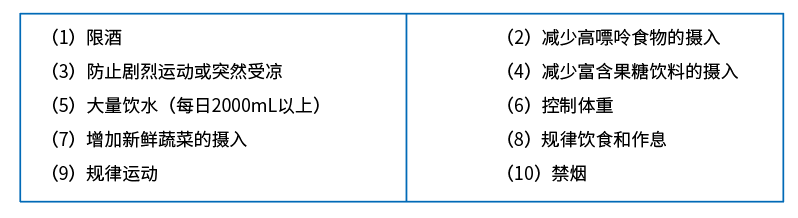
参考以上指南与专家共识,医学营养治疗推荐意见主要如下: 能量给予按标准体重计算,25~30kcal/(kg·d); 蛋白质0.8~1g/(kg·d),50~70g/d; 痛风急性发作时以植物蛋白为主,以免体内尿酸形成增加; 脂肪占总能量的20~25%,为40~50g/d; 碳水化合物占总能量的55~66%; 应注意供给B族维生素和维生素C; 痛风急性发作时,严格限制嘌呤摄入,并计算每日实际摄入嘌呤量,控制在小于150mg/d; 供给充足水分,液体量2000~3000ml/d,使每日尿量保持在2000ml以上,促使尿酸排出体外。
参考文献
[1] 中国医师协会中西医结合医师分会内分泌与代谢病学专业委员会,高尿酸血症和痛风病证结合诊疗指南( 2021-01-20),世界中医药,2021,16(2):183-188
[2] 李丹, 张剑勇. 痛风现代流行病学及降尿酸药物研究进展[J]. 风湿病与关节炎, 2016, 5(04):73-76.
[3] 康艺, 蒋力生. 饮食养生对痛风病的防治意义[J]. 江西中医药大学学报, 2019,31(3):14-16.
[4] 杨丽华,刘晓丽,蒋雅琼, 等.我国痛风的患病率及危险因素[J].医学研究杂志,2019,48(12):4-6,10.
[5] 韦慧艳,唐振柱,熊润松,等.高尿酸血症发生痛风的相关危险因素研究[J].应用预防医学,2018,11(12):110~111.
[6] Tsai EC, Boyko EJ, Leonetti DL, et al .Low sernnl testosterone level as a predictor of increased visceral fat in Japanese-American men[ J].Int J Obes Relat Metab Disord,2000,24(4):485-491.
[7] 朱君, 余俊文. 高尿酸血症和痛风的流行病学及其危险因素的研究进展[J]. 现代生物医学进展, 2008(01):201-205.
[8] 孙秀发, 凌文华. 临床营养学[M].北京:科学出版社, 2018:221-222.
[9] 齐玉梅, 郭长江, 田洪斌, 等. 现代营养治疗[M].北京:中国医药科技出版社, 2016:336.
[10] 孙秀发, 凌文华. 临床营养学[M].北京:科学出版社, 2018:222-223.
[11]Evans PL,Prior JA,Belcher J.et al. Obesity,hypertension and diuretic use as risk factors for incident gout: a systematic review and meta-analysis of cohort studies[J].Arthritis research &therapy,2018,20 ( 1) : 136.
[12] 王辰, 王建安, 黄从新, 等. 内科学(下册)[M].北京:人民卫生出版社, 2016:1229.
[13] 关大顺, 许先金, 关子安, 等. 现代代谢病与营养性疾病[M].天津:天津科技翻译出版公司, 2008:495-496.
[14] 王辰, 王建安, 黄从新, 等. 内科学(下册)[M].北京:人民卫生出版社, 2016:1230-1231.
[15] 齐玉梅, 郭长江, 田洪斌, 等. 现代营养治疗[M].北京:中国医药科技出版社, 2016:337.

- 【特康特食】肥胖症的流行病学、临床治疗及医学营养管理2021-08-04
- 【特康特食】阿尔兹海默症(AD)的流行学、临床治疗及医学营养管理2021-08-02
- 【特康特食】 癫痫的流行病学、临床治疗及医学营养管理2021-07-30
- 【特康特食】骨质疏松症的流行病学、临床治疗及医学营养管理2021-07-28
-
-
γ-氨基丁酸复合营养粉(盒装)
-
燕麦β-葡聚糖复合营养粉(盒装)





 鲁公网安备 37110502371159号
鲁公网安备 37110502371159号