【特康特食】阿尔兹海默症(AD)的流行学、临床治疗及医学营养管理
发表时间:2021-08-02

一、阿尔兹海默症的流行病学
阿尔兹海默症的概念
阿尔兹海默病(Alzheimer’s disease, AD)是以认知记忆障碍为主要特征的、 神经突触功能受损和渐进性神经元损伤的神经系统退行性疾病[1]。
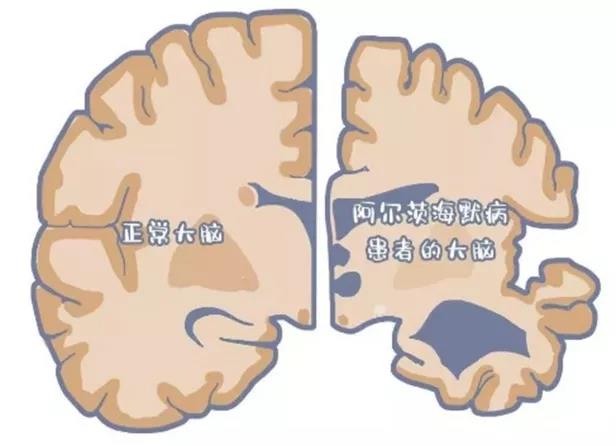
老年痴呆是一种起病隐匿的进行性发展的神经系统退行性疾病, 以记忆力下降、认知功能障碍、意识障碍、生活自理能力及社会活动能力下降甚至丧失为特征, 分为原发性和继发性两种[2]。其中,阿尔兹海默症是痴呆最常见的病因和最常见的老年期痴呆。

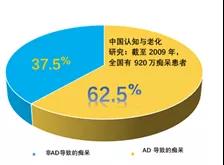
痴呆已经成为老年人群致死和致残的主要疾病之一, AD是痴呆的首要病因。根据我国流行病学调查显示, 65 岁及以上人群神经认知障碍(痴呆)总患病率为 5.14% -7.3%, 其中阿尔茨海默病(Alzheimer’s disease,AD)占50% -75%。 中国认知与老化研究(COAST研究)表明,截止到2009年, 中国有920万痴呆患者,其中62.5%的痴呆患者都是AD导致的[3]。
国际AD协会的相关报告指出,到2030年 AD患者预计达到7470万人次, 而到2050年将上升至1亿3150万人次,同时据我国2015年统计结果表明, 我国 AD患者已超过1460万,这说明 AD已然变为严重危害人类健康与生命安全的疾病之一[4-5]。
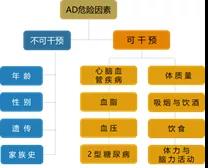
AD的危险因素《2018中国痴呆与认知障碍诊治指南(七): 阿尔茨海默病的危险因素及其干预》中将AD的危险因素分为可干预危险因素和不可干预危险因素。 其中,年龄和性别是AD公认的危险因素[6]。
流行病学研究显示,AD 的患病率随年龄增高而增高。 2009年太原市 9 个社区 5964 名≥65 岁老年人AD 患病率为4. 86%。其中,65-70岁AD患病率为1.92%, 70-75岁AD患病率为8.29%,75岁以上AD患病率为9.25% [7]。
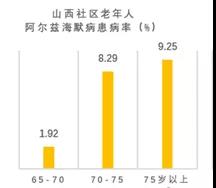
流行病学研究显示,AD 的患病率随年龄增高而增高。 2009年太原市 9 个社区 5964 名≥65 岁老年人AD 患病率为4. 86%。 其中,65-70岁AD患病率为1.92%,70-75岁AD患病率为8.29%,75岁以上AD患病率为9.25% [7]。
二、阿尔兹海默症的临床症状
阿尔兹海默症的起病较为隐匿或者缓慢,根据患者的认知能力和身体功能的恶化程度分为三个阶段。
1. 轻度痴呆期(1-3年)
主要表现为记忆减退(特别是新近发生的事情)、判断力下降、情感淡漠、言语减少、
出现时间定向障碍和视空间能力降低。
2. 中度痴呆期(2-10年)
表现为严重的记忆丧失、缄默、肢体僵直、日常生活不能自理、
大小便失禁、查体可见锥体束阳性、最终昏迷。
3.重度痴呆期(8-12年)
表现为严重的记忆丧失、缄默、肢体僵直、日常生活不能自理、
大小便失禁、查体可见锥体束阳性、最终昏迷。
三、阿尔兹海默症治疗方法
胆碱酯酶抑制剂:
是现今治疗轻中度AD的一线药物,主要包括多奈哌齐、卡巴拉汀、加兰他敏和石杉碱甲[9]。
兴奋性氨基酸受体拮抗剂:
盐酸美金刚是另一类AD治疗一线药物,对中重度AD患者妄想、激越等精神行为异常有一定治疗作用[9]。
中药及其他治疗药物:
银杏叶提取物(EGb 761)对AD、多发梗死性痴呆和轻度认知障碍(MCI)治疗有效,
可改善患者认知功能、日常生活能力及痴呆相关症状;为抗氧化剂维生素E可以延迟AD患者发病的进程[9]。
四.阿尔兹海默症的营养代谢与营养不良
能量代谢:
能量代谢异常是阿尔茨海默症高风险基础疾病的主要特征,能量代谢障碍会促进氧化应激和AD病理产物累积。
糖代谢:
在早期可表现为糖代谢的异常活跃,大脑对葡萄糖的利用率减低,
出现葡萄糖转运障碍及其在细胞内代谢障碍的发生。
同时,胰岛素水平的减低、中枢神经系统胰岛素作用的障碍以及胰岛素代谢通路抑制等因素发生,
导致胰岛素的抵抗以及缺失,进而引起糖代谢的异常,并最终导致AD的发生[10]。
脂代谢:
胆固醇水平升高促使Aβ迅速形成,形成炎症反应而损伤中枢神经,
最终形成阿尔茨海默病。血脂异常情况促进动脉粥样硬化形成后易演变为脑卒中等疾病,
从而加重了痴呆发病几率[11]。
维生素和矿物质:
钙、锌、铁、维生素K、维生素A在内的多种维生素和矿物质摄人显著低于同龄正常老年人,
血清叶黄素和β-胡萝卜素水平显著降低;血、脑脊液及脑组织中锌的含量均降低,
脑组织中硒、锌含量普遍下降,血清维生素C、维生素B、叶酸、锌水平显著低于同年龄段的健康人群。
五、阿尔兹海默病的营养支持治疗及指南
根据阿尔兹海默病患者的痴呆程度,选择合适的营养支持可以给予患者营养补充,维持各个器官组织的功能,特别是促进神经突触修复的营养物质,可延缓痴呆的病理过程。
增加优质蛋白质的供给。
每日摄入量以达到 1.0-1.2 g/kg 为宜,
按能量计算蛋白质摄入量占膳食总能量的 10% -15%,不宜超过20%,
且优质蛋白质的摄入量应占总蛋白质的摄入量 50%以上[13]。
减少脂肪及适量补充多不饱和脂肪酸和卵磷脂。
中国营养学会推荐成人脂肪摄入量一般控制在 20%- 30% 总能量摄入的范围内。
目前成人胆碱的参考摄入量为每日 500 mg,必需脂肪酸的摄入量,一般应不少于总能量的3%[13]。
减少碳水化合物的供给。
每日糖类供给以占总能量的55%-60% 为宜。老年人还应增加富含膳食纤维的食物[13]。
增加维生素的摄入。
AD 患者应注意供给维生素 E、维生素 C、B 族维生素等[13]。
抗氧化营养素如维生素E可以改善认知功能,B族维生素和膳食磷脂有助于神经细胞膜磷脂的合成。
适当增加矿物质
矿物质可以维持组织细胞渗透压,并维持神经和肌肉的兴奋性,
可适当增加钙、铁、锌、硒等的供应量,但要减少铝、铜、钠盐的摄入[13]。
参考文献
[1] 杜光, 胡俊波. 临床营养支持与治疗学[M]. 科学出版社, 2016.
[2] 王晓静, 魏树林, 初丽敏,等. 老年痴呆的早期诊断与治疗[J]. 临床合理用药杂志,
2015, 000(011):176-179.
[3] A J J, A F W, A C W, et al.
The prevalence of dementia in urban and rural areas of China[J].
Alzheimer's & Dementia,2014, 10(1):1-9.
[4]Abolhassani N ,Leon J, Sheng Z, et al.
Molecular pathophysiology of impaired glucose metabolism,
mitochondrial dysfunction,
and oxidative DNA damage in Alzheimer's disease brain[C]// Elsevier Ireland Ltd,
2017:95-104.
[5] Prince M, Wimo A, Guerchet M, et al.
World Alzheimer Report 2015: The Global Impact of Dementia.
An Analysis of Prevalence, Incidence, Cost and Trends[M].London:
Alzheimer’s Disease International,2015.
[6] 中国痴呆与认知障碍写作组, 中国医师协会神经内科医师分会认知障碍疾病专业委员会.
2018中国痴呆与认知障碍诊治指南(二):阿尔茨海默病诊治指南[J]. 中华医学杂志, 2018(1):971-977.
[7] 王艳平, 翟静波, 朱芳,等. 社区老年人阿尔兹海默病患病及影响因素分析[J].
中国公共卫生, 2011, 27(007):827-828.
[8] 杜光,胡俊波. 临床营养支持与治疗学[M]. 科学出版社, 2016.
[9] 中国痴呆与认知障碍写作组, 中国医师协会神经内科医师分会认知障碍疾病专业委员会.
2018中国痴呆与认知障碍诊治指南(二):阿尔茨海默病诊治指南[J]. 中华医学杂志, 2018(1):971-977.
[10] 赵琳琳,丁婧,曲扬.葡萄糖代谢异常与阿尔茨海默病发病机制的研究进展[J].
中国实验诊断学2020,24(6):1057-1059.
[11] 潘红珊,莫翠英,陈婉珉.糖脂代谢异常与阿尔茨海默病发病率的相关性[J].
青岛医药卫生 ,2016, 48(6):409-410
[12] 刘欣艳, 刘闻莺, 余雪君,等. 营养状况与阿尔兹海默病的相关性研究[J].
中国医药导报 2014,18: 62-65.
[13] 徐凤艳. 阿尔兹海默病的营养干预[J]. 沈阳医学院学报, 2013, 15(3):157-159.

- 【特康特食】肥胖症的流行病学、临床治疗及医学营养管理2021-08-04
- 【特康特食】阿尔兹海默症(AD)的流行学、临床治疗及医学营养管理2021-08-02
- 【特康特食】 癫痫的流行病学、临床治疗及医学营养管理2021-07-30
- 【特康特食】骨质疏松症的流行病学、临床治疗及医学营养管理2021-07-28
-
-
γ-氨基丁酸复合营养粉(盒装)
-
燕麦β-葡聚糖复合营养粉(盒装)





 鲁公网安备 37110502371159号
鲁公网安备 37110502371159号